Кетамин против опиоидов: кто быстрее поднимет настроение?
Следите за новостями по этой теме!
Подписаться на «Психология / Научные исследования»
Недавнее исследование, опубликованное в Журнале аффективных расстройств, обнаружило, что хроническое использование опиоидов может мешать мозгу генерировать плацебо-антидепрессивный ответ, но, похоже, не снижает эффективность кетамина. В повторном анализе данных из испытания 2023 года исследователи обнаружили, что пациенты, получавшие назначенные опиоиды, испытывали менее выраженное облегчение депрессии при получении плацебо, но показывали нормальный ответ при получении кетамина. Эти результаты указывают на возможное взаимодействие между опиоидными препаратами и естественными системами регулирования настроения в мозге и могут помочь исследователям лучше понять, как как препараты, так и ожидания влияют на психическое здоровье.
Мотивацией для этого исследования послужило неожиданное наблюдение. В недавнем испытании исследователи рассматривали, может ли кетамин все еще производить антидепрессивные эффекты, даже когда его психоактивные эффекты были устранены с помощью общей анестезии. Удивительно, но пациенты, получившие плацебо во время операции, испытали улучшение депрессии, почти равное тем, кто получил кетамин.
«В 2023 году мы опубликовали удивительный результат из исследования о антидепрессивном эффекте кетамина. В этом исследовании мы пытались 'убрать поездку' из кетамина, вводя его депрессивным пациентам, которые получали общую анестезию для операции», - объяснил автор исследования Борис Д. Хейфетс, доцент анестезиологии, пероперативной и болевой медицины в Стэнфорде. «Это исследование было спроектировано как действительно слепое, в том смысле, что участники не знали, какое лечение они получили (что редко встречается в исследованиях с психоделическими препаратами) и было нацелено на проверку идеи, что кетамин может иметь антидепрессивные эффекты независимо от своих острых психоактивных эффектов.»
«Мы обнаружили, что пациенты, получившие кетамин под анестезией, чувствовали себя очень хорошо (>50% ответа на лечение, ~30% ремиссия от депрессии). Мы также обнаружили, что группа плацебо добилась аналогичных результатов - на самом деле, не было разницы между кетамином и плацебо, что некоторые восприняли как то, что кетамин не лучше плацебо.
«Для меня и для Терезы Лий, ведущего автора обоих, самым интересным результатом было мощное влияние плацебо, которое предполагает, что когда вы создаете большие ожидания (как это часто делается в психоделических исследованиях), но никогда не испытываете 'момент предательства', когда участники понимают, что получили плацебо, вы можете добиться мощных и, возможно, долговременных антидепрессивных эффектов. Это новое исследование, опубликованное в прошлом месяце, является повторным анализом наших данных 2023 года и более детально рассматривает эффект плацебо.»
Опиоиды, такие как морфин и оксикодон, активируют опиоидные рецепторы мозга и широко используются для лечения хронической боли. Кетамин, первоначально разработанный как анестетик, в последние годы привлек внимание благодаря своим быстрым антидепрессивным эффектам. Оба, опиоиды и кетамин, похоже, влияют на настроение через пути, вовлекающие эндогенную опиоидную систему мозга — сеть, которая помогает регулировать боль, удовольствие и эмоциональные реакции. Предыдущее исследование показало, что эта система также может играть роль в ответах на плацебо, включая те, которые наблюдаются в антидепрессивных испытаниях.
Поскольку хроническое использование опиоидов может изменять чувствительность опиоидной системы, исследователи задались вопросом, уменьшает ли такое использование плацебо-ответ у депрессивных людей. Чтобы проверить эту идею, Хейфетс и его коллеги повторно проанализировали данные из исследования 2023 года с участием 40 взрослых с крупным депрессивным расстройством, проходящих плановую операцию под общей анестезией. Половина участников получила одиночную внутривенную дозу кетамина, в то время как другая половина получила солевой плацебо. Затем исследователи оценили симптомы депрессии с использованием шкалы депрессии Монтгомери-Асберга (MADRS) в течение двух недель после лечения.
В этом новом анализе участники были классифицированы в зависимости от того, использовали ли они назначенные опиоидные препараты в момент скрининга. Из 40 участников 16 были пользователями опиоидов. Важно, что люди, принимающие высокие дозы опиоидов или препараты, действующие иначе на опиоидные рецепторы, были исключены. Уровни боли до и после операции измерялись, чтобы убедиться, что любые изменения настроения не были просто следствием различий в физическом дискомфорте.
Анализ показал, что пациенты, принимающие опиоиды в начале исследования, испытали меньшие улучшения симптомов депрессии после получения плацебо. В среднем их показатели MADRS упали значительно меньше, чем у пользователей не опиоидов, что указывает на более слабый плацебо-ответ. В то же время среди пациентов, которые получили кетамин, не было значимых различий в результатах депрессии между пользователями опиоидов и не пользователями.
Эти результаты указывают на то, что "долгосрочное использование опиоидов может мешать плацебо-антидепрессивному ответу". Хейфетс сказал PsyPost: "Эндогенные опиоиды (такие как 'эндорфины') известны своей ролью в плацебо-аналгезии, но до сих пор не так много известно о плацебо-антидепрессивном ответе. Это исследование предполагает, что эти разные типы плацебо-ответов могут делиться одним механизмом."
Чтобы укрепить свои результаты, исследователи провели несколько тестов чувствительности. Они использовали альтернативный метод самооценки депрессии, известный как Шкала тревожности и депрессии в больнице (HADS), который включает как элементы настроения, так и тревожности и часто используется в больничных условиях. Результаты по HADS подтвердили начальную находку: подавляющий эффект употребления опиоидов на плацебо-ответ становился более выраженным со временем, в то время как такого эффекта не наблюдалось с кетамином.
Важно, что команда исключила боль как вероятное объяснение своих находок. Существовала очень небольшая корреляция между сообщаемым уровнем боли у пациентов и их симптомами депрессии после лечения. Даже несмотря на то, что пользователи опиоидов, как правило, сообщали о большем послеоперационном болевом пороге, это не объясняло их уменьшенный плацебо-ответ.
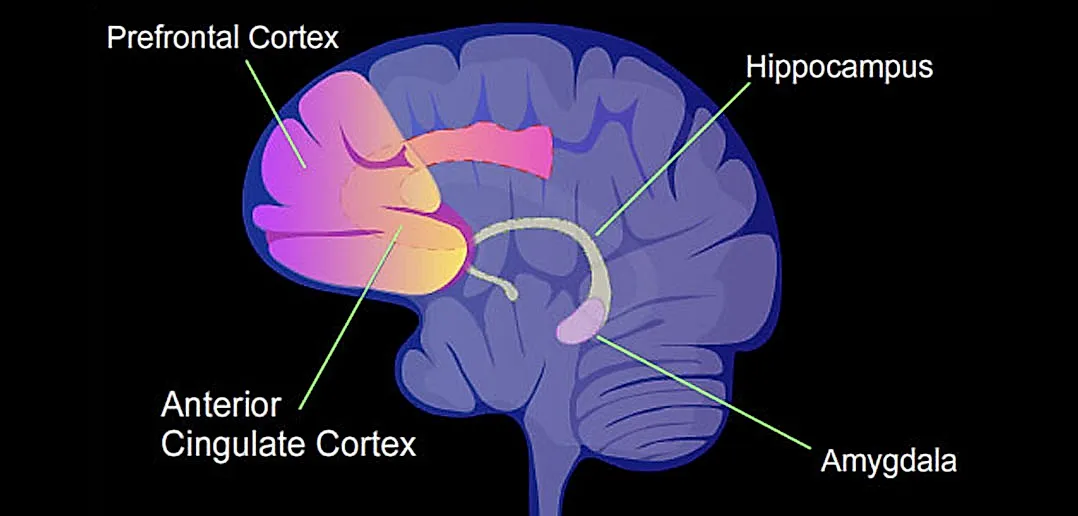
Так почему употребление опиоидов ослабляет реакцию мозга на плацебо, но не на кетамин? Одна из возможностей заключается в том, что хроническое воздействие опиоидных препаратов может десенсибилизировать или нарушить естественную опиоидную систему организма. Поскольку считается, что эта система играет роль в эффекте плацебо, такие изменения могут уменьшить способность человека испытывать улучшения настроения только от положительных ожиданий. Напротив, кетамин может работать через механизмы, которые обходят или даже восстанавливают эти изменения, связанные с опиоидами, восстанавливая чувствительность мозга к сигналам, регулирующим настроение.
"Эффект плацебо - это сложный и мощный ответ с биологическим механизмом", - сказал Хейфетс. "Кетамин может действовать, 'сбрасывая' чувствительность к плацебо. Мы и другие предложили, что психоделические препараты, такие как кетамин, могут работать через те же биологические пути, что и плацебо. Как вы можете представить, это затрудняет разграничение, что является 'плацебо', а что - 'эффект препарата' в психоделических испытаниях - этот вопрос стал большой проблемой для исследований с такими препаратами, как псилоцибин и MDMA."
Исследователи признали некоторые ограничения. Это был пост-хок анализ, что означает, что исследование не было изначально спроектировано для изучения эффекта опиоидов в частности. Размер образца был мал - всего 7 пользователей опиоидов в группе плацебо и 9 в группе кетамина, что увеличивает вероятность статистического шума. Исследователи также не имели точных данных о том, насколько строго участники следовали своим предписанным режимам приема опиоидов или когда они в последний раз принимали свои лекарства перед исследованием.
"Это был повторный анализ небольшого исследования", - отметил Хейфетс. "Это далеко от доказательства идей, которые мы выдвигаем, но это поддерживает некоторые новые мысли о том, как работают психоделические препараты, и о том, как работают сильные плацебо-эффекты."
Несмотря на эти ограничения, результаты поднимают важные вопросы о том, как распространенные лекарства, такие как опиоиды, могут мешать как лекарственным, так и плацебо-базированным лечениям депрессии. Многие люди с депрессией также получают назначение опиоидов, и это несоответствие получило относительно небольшое внимание в клинических исследованиях. Если опиоиды подавляют естественные плацебо-ответы мозга, то они могут невольно уменьшить эффективность как экспериментальных, так и стандартных методов лечения.
Авторы предлагают, чтобы будущие исследования непосредственно изучали, как воздействие опиоидов - как краткосрочное, так и долгосрочное - взаимодействует с результатами лечения в антидепрессивных испытаниях. Они также предлагают, что инструменты, такие как антагонисты опиоидов (которые блокируют опиоидные рецепторы), могут быть использованы для изучения путей плацебо мозга и лучшего понимания того, как взаимосвязаны ожидания, нейрохимия и реакции на лечение.
Эти findings также имеют значение для проектирования клинических испытаний, особенно в развивающейся области психоделической терапии. Традиционные двойные слепые исследования часто испытывают трудности в разделении эффектов препарата и эффектов ожидания, когда рассматриваются изменяющие сознание вещества, такие как кетамин или псилоцибин. Если сами плацебо-ответы могут быть использованы и регулированы через биологические системы, это могло бы открыть двери для более персонализированных и эффективных методов лечения, даже тех, которые не полагаются исключительно на фармакологию.
"Одна из основных проблем в изучении психоделических терапий заключается в том, что классическое 'рандомизированное двойное слепое испытание' не работает должным образом - участники обычно знают, что они получили, и попытки запутать участников относительно того, что они получили, могут работать против одной из номинальных целей психоделической терапии, которая заключается в получении инсайта о своем состоянии и о себе", - объяснил Хейфетс. "Мы думаем, что понимание механизма плацебо даст нам представление о том, как максимизировать потенциальные преимущества психоделиков."
Исследование под названием «Опиоиды снижают плацебо-антидепрессивный ответ: наблюдательные пост-хок находки из рандомизированного контролируемого испытания с кетамином» было написано Терезой Р. Лий, Джозефиной Р. Флоры, Робином Л. Окада, Лизой Дж. Чианфичи, Лаурой М. Хак, Аланом Ф. Шатцбергом и Борисом Д. Хейфетсом.
PEREC.RU
Научный мир снова ослепителен: исследование о плацебо и антидепрессантах не оставляет шансов на обыденное восприятие. В этот раз под прицелом — опиоиды и их магическая способность шутить с нашим настроением. Взглянем, как под этой завесой умных слов прячется режиссура интересов.
Проблема ясна: хроническое использование опиоидов мешает мозгу верить в чудеса плацебо, но на кетамин — он не так прост. То ли это эгоизм фармацевтических гигантов, то ли просто некомпетентность, но в великой схеме "плацебо" внезапно обнаружили недостатки. Изучите статистику — 40 человек, 16 опиоидов, и вот оно: пожалуйста, ваши плацебо не работают так, как предполагалось.
Лоббисты фармакологической индустрии, очевидно, диктуют условия игры: вот вам научное открытие, вот вам новая волна исследований. Кто-то хочет заработать на антагонистах опиоидов, чтобы снова представлять их как спасителей. И, конечно, опиоиды-злодеи, которые, как ни старайся, улучшают состояние только предвкушением, но не фактически.
Всё это напоминает цирк — исследователи, сами того не зная, становятся постановщиками представления. Под общим названием "плацебо" прячутся сложные механизмы, которые фармацевты с завидным спокойствием изучают, пока пациенты сидят в ожидании чуда. Никто не удивится, если в следующем выпуске найдем рекомендации о том, как опиоиды могут улучшить продажи кетамина.
Научная честность здесь, конечно, под вопросом. Кто рискнул бы испортить свой бизнес-договор с компаниями, производящими опиоиды и антагонисты? Высокая наука сталкивается с несколькими «но», и каждый из них затихает под тяжестью финансовых интересов. Обычно довольно сложно разобрать, где заканчивается исследование и начинается реклама.
Несмотря на аккуратный подход к плацебо, результаты, увы, не далеки от клинической неразберихи. Платная экспериментальная работа с кетамином может быть лишь хорошо продуманным маркетинговым ходом; результат — хорошая статья и новые гранты. И кто знает, может, через год мы увидим сообщения о «внезапной эффективности» опиоидов на плацебо на фоне эффективности кетамина — всё для блага общества.
Но исключительно для науки и блага пациентов! Как трезво всё выглядит в мире, где фармацевтический маркетинг решил взять правление в свои руки. Так что, продолжайте мечтать, дорогие исследователи — ваш плацебо-ответ будет переведен в банке с бон диетической таблеткой, настоятельно рекомендующейся некоторыми не до конца опьянёнными «экспертами».