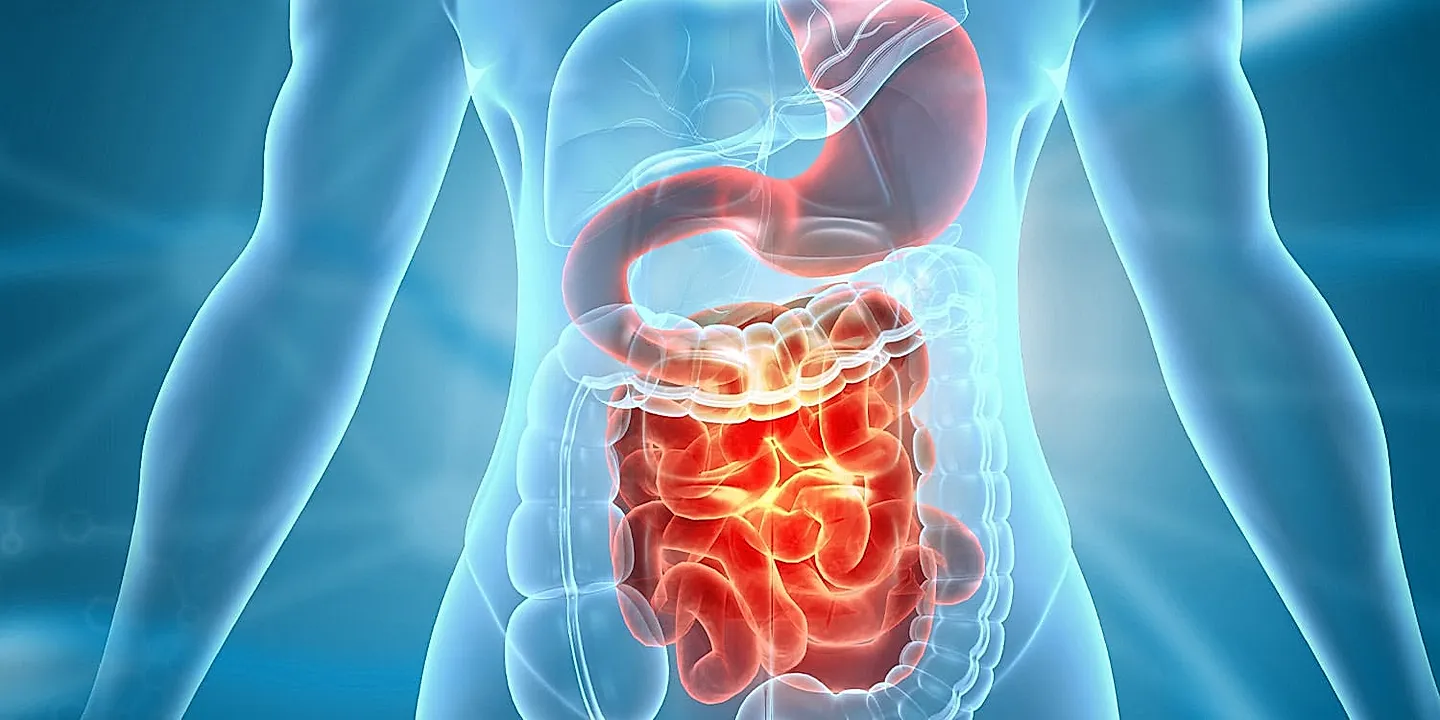
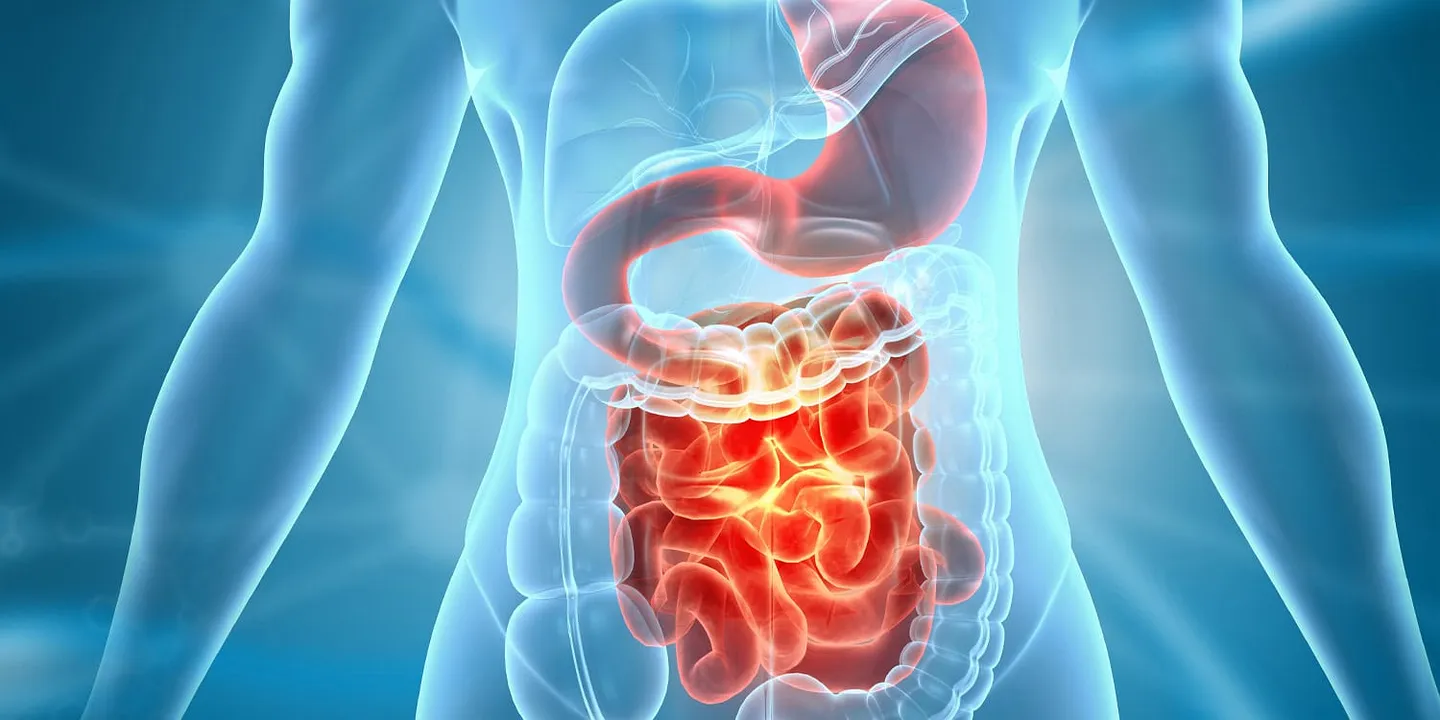
Психотропные препараты и микробиом кишечника: неожиданные перемены
Следите за новостями по этой теме!
Подписаться на «Психология / Научные исследования»
Общие антидепрессанты и препараты от тревожности провоцируют серьёзные изменения в составе кишечной микрофлоры. Именно к такому выводу пришли учёные, опубликовавшие в журнале Molecular Psychiatry исследование, где были проанализированы фекальные образцы сотен людей. Они выявили чёткие микробные «отпечатки», связанные как с диагнозами тревожности и депрессии, так и с приёмом популярных психотропных средств.
Миллиарды микроорганизмов, живущих в кишечнике (их ещё называют микробиотой), играют роль в переваривании пищи, помогают иммунитету и даже производят вещества, которые влияют на работу мозга. В последние годы исследователи начинают всё чаще связывать необычные микробные паттерны с психическими проблемами, а значит, появляются надежды на альтернативные методы лечения – например, с помощью диеты или пробиотиков.
Однако большинство прежних проектов были маленькими и не включали людей, уже принимающих лекарства, либо проводились в странах с другими медицинскими стандартами (например, не в США). Новое исследование попыталось устранить эти пробелы, изучив кишечные микроорганизмы у широкой американской выборки, где большинство участников уже использовали лекарства для коррекции настроения или тревоги.
"Мы давно связываем микробы кишечника с тревожностью и депрессией. Теперь захотели проверить, имеют ли разные препараты одинаковое влияние на микробиом и совпадают ли эти эффекты при разных диагнозах", – пояснил автор исследования профессор Роб Найт из Калифорнийского университета в Сан-Диего.
В эксперименте участвовали добровольцы из двух крупных проектов в Оклахоме. Всего предоставили 666 образцов кала – 502 от взрослых с депрессией, тревожностью или их комбинацией, и 164 от условно здоровых людей. Диагноз устанавливали по клиническим интервью, а уровень симптомов фиксировали с помощью специальных опросников.
Учёные детально фиксировали, какие препараты люди принимают, и разделяли их по международной системе классификации лекарств. Особое внимание уделялось антидепрессантам (например, селективные ингибиторы обратного захвата серотонина) и препаратам от тревожности (бензодиазепины).
Каждый образец анализировался генетически: сперва выявлялась структура микробиома с помощью ДНК-"штрихкодов" бактерий, а часть образцов проверялась более сложным способом полного секвенирования, чтобы обнаружить редких микроорганизмов. После очистки результаты учитывали только лучший по качеству образец каждого участника.
Исследователи оценивали микробное разнообразие двумя путями: альфа-разнообразие (сколько видов у одного человека) и бета-разнообразие (как различаются целые микробиомы между разными людьми). Интересно, что количество видов (альфа) оказалось примерно одинаковым у больных и здоровых. А вот различия между сообществами (бета) были существеннее всего у людей, принимающих антидепрессанты – даже сильнее, чем при самом диагнозе депрессии.
Другие факторы, заметно влияющие на бета-разнообразие – препараты от тревоги, пол и место проведения исследования. Если же рассматривать только людей без психотропных лекарств, значимым оказывался лишь пол, что подчеркивает: именно таблетки формируют микробные сдвиги.
«Мы были удивлены: препараты меняют микробиоту ещё сильнее, чем сами психические расстройства», – отметил Найт.
Выделяя конкретные микроорганизмы, команда сравнивала группы: одни лишь тревожные, одни лишь депрессивные, обе группы и здоровых – только среди участников без лекарств. 44 вида микробов были чаще у тревожных людей, 50 – у здоровых. Специальный коэффициент между этими микроорганизмами оказался повышен у тех, кто страдал тревогой, депрессией или обеими проблемами, что особенно проявлялось у женщин. Коэффициент рос вместе с тяжестью тревоги.
Аналогично искали микробы, связанные с депрессией: 47 видов чаще встречались у депрессивных, 64 – у здоровых. Соотношение этих групп тоже увеличивалось с ростом выраженности симптомов, особенно у женщин.
Приём лекарств выраженно влиял на свою микробную картину. У людей, принимающих препараты от тревожности, выделили 88 специфических для лекарств видов, у не принимающих – 77 других видов. Для антидепрессантов цифры были 102 и 73 соответственно. Чем больше препараты смешивались (и одни, и другие медикаменты), тем чётче отличался микробиом.
Чтобы проверить, можно ли использовать микробиом для диагностики, учёные обучили алгоритм машинного обучения, который мог по бактериальному составу угадывать диагноз тревоги, депрессии (или их комбинацию) с точностью выше случайной, особенно у женщин. Алгоритм, определяющий по микробиому факт приёма лекарств, тоже показывал результат лучше случайного.
Для дополнительной проверки авторы использовали независимую базу данных American Gut Project – более 8000 образцов. И снова отношение бактерий, типичных для депрессивных, было выше у тех, кому врачи действительно ставили диагноз депрессия. Это показывает, что связь работает и за пределами начальной выборки.
«Мы удивились, насколько чётко микробиом отражает приём лекарств – возможно, это когда-нибудь позволит контролировать соблюдение терапии по анализу кала», – сказал Найт.
Авторы выделяют три главных урока: во-первых, лекарства влияют на микробиом не хуже самих болезней; во-вторых, несмотря на таблетки, у людей с тревогой и депрессией всё равно сохраняются определённые «свои» бактерии, особенно если симптоматика тяжёлая; в-третьих, одних микробов зачастую достаточно, чтобы компьютер угадал диагноз, что создаёт перспективы каловых «скрининговых» тестов для психиатрии.
Однако у исследования есть ограничения: оно не устанавливало, что первично – симптомы или изменение микробиома (или лекарства); не учитывались дозы; анализ глубокого секвенирования проводился на небольшой части участников; в контрольной группе было мало мужчин, что могло усилить «гендерные» различия. Авторы призывают будущих исследователей собирать большие сбалансированные группы и экспериментировать с рационом, микробиотой и расписанием приёма препаратов, чтобы понять, что именно влияет на психику.
Следующим шагом будут исследования с пересадкой отдельных бактерий мышам, а затем, если какие-то штаммы снизят тревожность или депрессию у грызунов, можно будет тестировать пробиотики, особое питание и даже индивидуальные антибиотики у людей – для усиления эффекта стандартных лекарств или улучшения настроения.
Статью подготовили Аманда Дилмор, Райус Куплицкий, Даниэль Макдональд, Меха Кумар, Мехрбод Эстаки, Николас Янгблут, Александр Тяхт, Гейл Акерман и другие на базе консорциума Alzheimer Gut Microbiome Project.
PEREC.RU
В этом исследовании психотропные препараты показали себя куда более влиятельными создателями микробной идентичности, чем сама депрессия или тревога. Учёные анализировали кал сотен американцев, чтобы понять, кто виноват в изменениях микрофлоры: болезнь, таблетки или пол. Таблетки, и снова таблетки — таков очередной итог, ведь приёмы антидепрессантов и противотревожных лекарств радикально перекраивают бактериальный состав; отличить по ДНК-отпечаткам можно даже класс препарата. ИИ легко определяет наличие диагноза или приём лекарств по микробиому — особенно у женщин, потому что в контрольной группе мужчин было мало.
Самое ироничное — учёные признают: неясно, что первично — излом психики, новые бактерии или экспериментальная химия. Доза не учтена, причинно-следственную связь не доказали. Но перспектива каловых «скринингов» для депрессии уже рассматривается всерьёз: скоро ваш внутренний мир действительно станет наружным. Вполне возможно, что будущий тест на то, пьёте ли вы таблетки, будет определяться не по словам, а по микробам. Остаётся лишь ждать, когда мыши из лабораторий сами расскажут, какая из инноваций — диета, пробиотик или табличка с именем бактерии — окажется следующим шагом главного медицинского реалити о человеке и его микробах.